復星醫藥自研藥蘆沃美替尼臨床研究更新數據亮相ASCO年會
2025年5月22日,美國臨床腫瘤學會(ASCO)年會公佈了入選研究摘要。由復星醫藥自主研發的蘆沃美替尼片(FCN-159)治療兒童I型神經纖維瘤病相關叢狀神經纖維瘤(NF1相關PN)的2期臨床研究更新數據入選1。
蘆沃美替尼片是一款高選擇性MEK1/2抑制劑,其雙適應症(朗格漢斯細胞組織細胞增生症和組織細胞腫瘤、I型神經纖維瘤病相關叢狀神經纖維瘤)在獲CDE多次突破性治療和優先審評認定後,已於5月29日獲批上市。
基於該研究在2023年及2024年ASCO年會已公佈的1/2期研究數據,本次數據更新了最新隨訪的療效和安全性數據,展示了蘆沃美替尼積極的臨床獲益和良好的安全性,將為蘆沃美替尼的科學治療再添力證。

聚焦NF1兒童困境,填補治療空白
I型神經纖維瘤病(NF1)是一種常染色體顯性遺傳性腫瘤性疾病,常累及多系統。約30%-50%的患者伴發叢狀神經纖維瘤(PN),可導致毀容、疼痛、身體功能障礙等嚴重問題並顯著影響患者生活質量。PN患者大多在幼年時期起病,且在生長發育關鍵的兒童期疾病進展更為迅速,因此兒童NF1-PN的治療需求尤為迫切2。
目前手術雖為NF1相關PN的主要治療手段,但因為瘤體起源於神經,約只有15%的患者腫瘤可完全切除,43%的患者術後會出現PN復發3。不可切除或術後復發的PN患者治療選擇極為有限,尤其是對於2歲的中國兒童患者,在蘆沃美替尼獲批前無藥物可用。
本研究為一項多中心,開放標籤2期臨床試驗。其主要目的是評估蘆沃美替尼片(FCN-159)治療兒童I型神經纖維瘤病相關叢狀神經纖維瘤(NF1相關PN)的有效性及安全性。主要終點為研究者評估的客觀緩解率(ORR),關鍵次要終點為盲態獨立評審委員會(BIRC)評估的ORR。
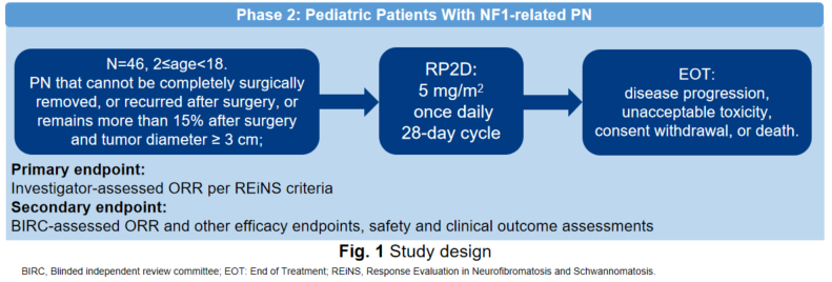
蘆沃美替尼起效迅速且療效顯著,ORR達60.5%,中位起效時間為4.7個月
截至2024年9月23日,本項多中心,開放標籤2期臨床研究納入46例2-18歲(不含)NF1相關PN兒童患者接受蘆沃美替尼(5 mg/m2,每日一次)治療。中位隨訪時間為25.1個月。
在43例可評估患者中,研究者評估且確認的客觀緩解率(ORR)達60.5%(95% CI:44.4-75.0),26例達到部分緩解(PR),17例疾病穩定(SD),無患者疾病進展。中位緩解持續時間(DOR)和中位無進展生存期(PFS)未達到。
在43例可評估患者中,BIRC評估且確認的ORR為44.2%(95% CI:29.1-60.1),19例達到PR,24例達到SD,無患者疾病進展。
研究者評估的中位起效時間為4.7個月,BIRC評估的中位起效時間位5.5個月。
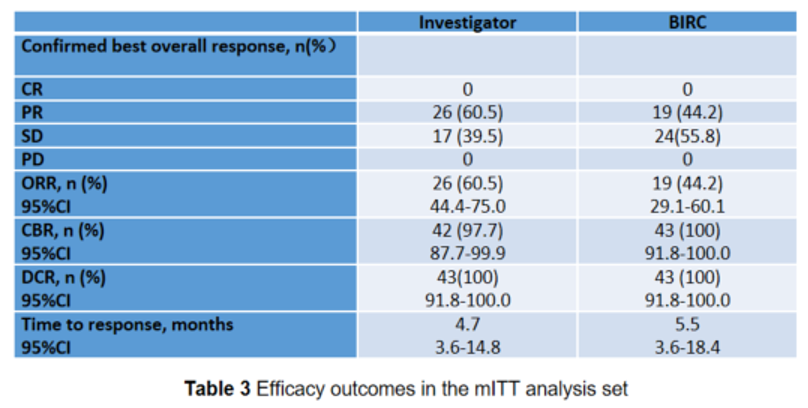
基線NRS≥2分患者中,92.9%疼痛明顯改善
在14例可評估疼痛的患者中(即基線總體腫瘤疼痛評分≥2且至少有一次基線後評估的患者),與基線相比,中位最大疼痛降低分數的變化為-3.5分。13例(92.9%)患者的疼痛評分至少降低2分,達到了臨床意義的改善。11例(78.6%)患者的疼痛評分為0,即疼痛完全消失。
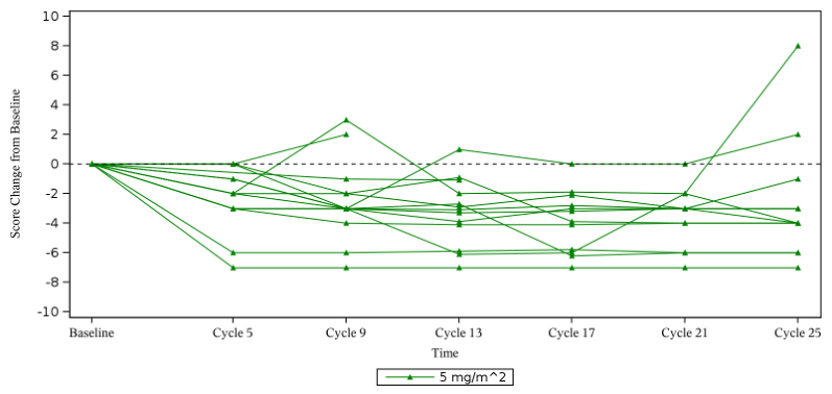
安全性良好,不良事件多為1-2級且可控,未出現新的安全性信號
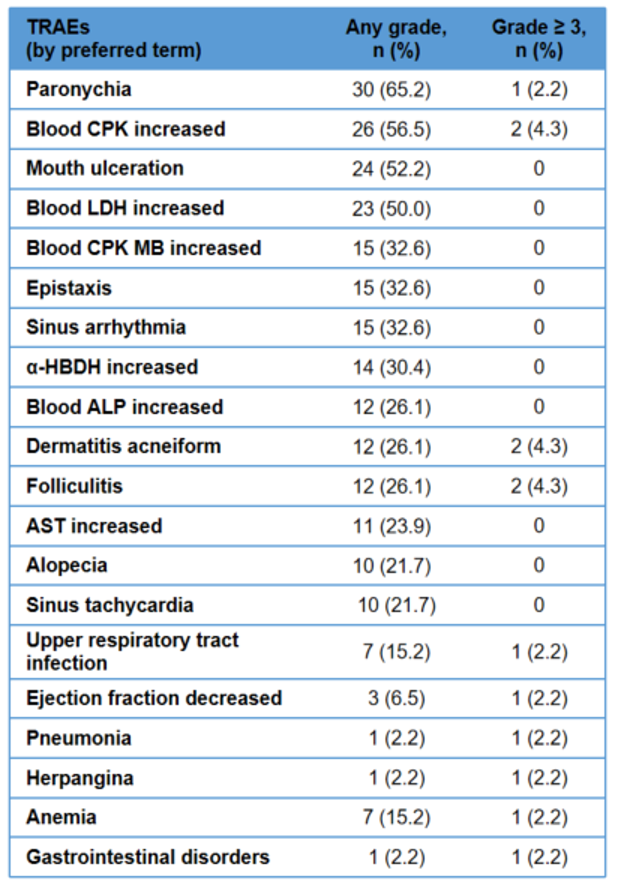
與研究藥物有關的不良事件(TRAEs)發生率為97.8%,以1-2級為主,≥3級TRAEs僅佔21.7%,常見不良事件主要包括甲溝炎(65.2%)、血肌酸磷酸激酶(CPK)升高(56.5%)、口腔潰瘍(52.2%)和血乳酸脫氫酶升高(50%),均為MEK抑制劑類藥物常見可控性反應。
腹痛、腹瀉、噁心和嘔吐的發生率在2.2%至19.6%之間,且均未達3級。僅2例(4.3%)患者出現與研究藥物有關的嚴重不良事件(痤瘡樣皮炎和感染性肺炎)。13例(28.3%)患者出現導致暫停用藥的TRAE,無TRAE導致劑量降低、永久停藥或死亡。患者依從性達到100%。
蘆沃美替尼的安全性良好,不良事件經過對症治療和暫停用藥後可有效管理。在兒童及青少年中耐受性良好。
代謝穩定、高選擇性、低毒性的特點,為中國NF1患兒帶來臨床獲益
作為首個國產MEK抑制劑,蘆沃美替尼在結構上通過協同設計,實現了代謝穩定、高選擇性和低毒性,以及半衰期延長的優勢。藥代動力學特徵支持藥物每日給藥1次,不受餐食影響並具有更少的合併用藥影響,均帶來更好的依從性,適合兒童長期用藥。蘆沃美替尼不僅以高選擇性機制突破了傳統治療的局限性,更通過顯著的腫瘤緩解率與疼痛改善數據,將為NF1患兒帶來積極的臨床獲益。
此外,蘆沃美替尼片用於治療成人Ⅰ型神經纖維瘤病於中國境內處於Ⅲ期臨床試驗階段,該藥品用於低級別腦膠質瘤、顱外動靜脈畸形、兒童朗格漢斯細胞組織細胞增生症的治療於中國境內均處於Ⅱ期臨床試驗階段,其中,該藥品用於無法手術或術後殘留/復發的NF1相關的叢狀神經纖維瘤成人患者、兒童朗格漢斯組織細胞增生症兩項適應症均已被國家藥監局藥品審評中心納入突破性治療藥物程序。復星醫藥將持續推進蘆沃美替尼片在其它適應症的開發,為更多患者帶來福音。
*本材料為專業醫學資料,僅供醫療衛生專業人士參考,具體診療信息請遵醫囑。
參考文獻:
1. JinHu Wang et al. JCO 43, 10044-10044(2025).
2.中國罕見病聯盟Ⅰ型神經纖維瘤病多學科診療協作組. [J].罕見病研究, 2023,2(2):210-230.
3. Fisher MJ, et al. Neuro Oncol. 2022;24(11):1827-1844